บทนำ
การปลูกถ่ายไขกระดูก (Bone marrow transplantation) รักษาผู้ป่วยโดยใช้เซลล์ต้นกำเนิดเม็ดโลหิต (Hematopoietic stem cell) จากพี่น้องที่มีหมู่เนื้อเยื่อ HLA (Human leukocyte antigen) ตรงกัน เป็นที่ยอมรับในวงการแพทย์ว่า เป็นวิธีการที่ประสบความสำเร็จในการรักษาเด็กและผู้ใหญ่ที่ป่วยเป็นโรค อันตรายหลายชนิด อาทิเช่น โรคมะเร็งที่มีความเสี่ยงหรือมีโอกาสกำเริบสูง โรคภูมิคุ้มกันบกพร่องแต่กำเนิด โรคทางเมตาบอลิค โรคไขกระดูกฝ่อหรือทำงานผิดปรกติ โชคไม่ดีที่ผู้ป่วยที่จำเป็นต้องรับการปลูกถ่ายส่วนใหญ่ ไม่มีพี่น้องหรือเครือญาติที่มีหมู่ HLA ตรงกัน ถึงแม้ว่าการก่อตั้งโครงการขึ้นทะเบียนอาสาสมัครผู้บริจาคไขกระดูก (National Marrow Donor Program)1,2 ที่สหรัฐอเมริกา จะมีมาตั้งแต่ปี พ.ศ. 2529 และจากนั้นจะมีการตั้งโครงการดังกล่าว ในแต่ละประเทศที่พัฒนาแล้วทั่วโลก แต่ก็ไม่สามารถสรรหาผู้บริจาคไขกระดูกหรือ stem cell ที่เหมาะสมให้ผู้ป่วยได้ทุกราย3 ดังนั้น ในช่วง 10 กว่าปีที่ผ่านมา แพทย์และผู้วิจัยทางคลินิคจึงได้วิเคราะห์ศึกษาความเหมาะสมของการนำ stem cell จากเลือดสายสะดือและรก มาเป็นทางเลือกใหม่ในการปลูกถ่าย4 ท่ามกลางความก้าวหน้าพัฒนาทางการแพทย์อย่างไม่หยุดยั้ง ด้วยประสบการณ์วงการแพทย์ในปัจจุบัน ถือว่าการปลูกถ่ายเลือดสายสะดือเป็นทางเลือกที่สำคัญ ในกรณีที่แพทย์ไม่สามารถเสาะหาผู้บริจาคไขกระดูกที่เหมาะสมกับผู้ป่วยได้
การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดโลหิตโดยใช้เลือดจากสายสะดือและรก (Umbilical cord blood stem cell transplantation)
เซลล์ ต้นกำเนิดเม็ดโลหิตจาก cord blood เป็นแหล่งทางเลือกใหม่ในการแสวงหาเซลล์เพื่อใช้ในการปลูกถ่ายแบบ allogeneic โดยเฉพาะอย่างยิ่งเป็นประโยชน์แก่ผู้ป่วยที่ไม่มีพี่น้องที่ HLA ตรงกัน ข้อจำกัดของการปลูกถ่ายไขกระดูกหรือ peripheral blood stem cell แบบ allogeneic แต่เดิมคือ การขาด HLA-matched donors ที่เหมาะสม และภาวะแทรกซ้อน graft-versus-host disease (GVHD) ซึ่งถ้ามีความแตกต่างกันของ HLA (HLA disparity) ระหว่างผู้ให้ (ผู้บริจาค) และผู้รับ (ผู้ป่วย) มากเท่าไร โอกาสที่จะเกิด GVHD และมีอาการรุนแรง จะมากขึ้นเท่านั้น ในกรณีที่ผู้ป่วยไม่มีพี่น้องที่เป็น HLA-identical แพทย์อาจจะต้องเลือกใช้ผู้บริจาคที่เป็นพี่น้องหรือเครือญาติผู้ป่วยที่เป็น partially-mismatched หรือไม่ก็ใช้อาสาสมัครผู้บริจาค (unrelated, volunteer donor) ที่ matched ผลการรักษาด้วยการปลูกถ่ายเซลล์ต้นกำเนิดดีขึ้นตามลำดับจากอดีตจนถึง ปัจจุบัน นั่นเป็นเพราะความก้าวหน้าในการตรวจ HLA typing ถึงระดับ molecular ทำให้ตรวจ major HLA antigen คือ HLA-A, -B, -DR ทั้ง 6 ตำแหน่งของผู้ป่วยและผู้บริจาคได้ match กันดีขึ้น แต่อย่างไรก็ตาม การที่สามารถตรวจ high-resolution molecular typing ได้อย่างละเอียดแม่นยำขึ้น ก็ทำให้ลดโอกาสที่จะพบผู้บริจาคที่มี HLA-identical ทั้ง HLA-A, -B, -C, -DR, -DQ, และ -DP อย่างสมบูรณ์จริงๆ5-9
ตั้งแต่ การปลูกถ่าย Allogeneic umbilical cord blood transplantation ประสบความสำเร็จเป็นครั้งแรกในโลกเมื่อปี พ.ศ. 2531 ซึ่งเป็นการรักษาผู้ป่วยเด็กโรค Fanconi anemia10 โดยใช้ cord blood ของน้องผู้ป่วยเอง (related donor) ก็มีการพัฒนาจัดตั้งธนาคารเลือดจากสายสะดือ (Cord blood banks) และการปลูกถ่ายเพิ่มขึ้นตามลำดับทั่วโลก สิ่งที่วงการแพทย์ได้เรียนรู้จากความสำเร็จนี้คือ การเก็บ umbilical cord blood unit สามารถกระทำได้เมื่อทารกแรกเกิดคลอดและตัดสายสะดือแล้ว โดยไม่มีอันตรายต่อตัวทารกแรกเกิดเลย, Cord blood stem cells สามารถถูกเก็บสงวนแช่แข็งไว้ (cryopreservation) สามารถนำกลับมาอุ่นให้อยู่ในสภาพของเหลว (thawing) และนำมาปลูกถ่ายติดสำเร็จ (engraftment) ในตัวผู้ป่วยได้, และ cord blood เพียง unit เดียวอาจมีจำนวน stem cell เพียงพอที่จะฟื้นฟู (reconstitution) ระบบ lympho-hema topoiesis ของผู้ป่วยที่เป็นเด็กหรือผู้ที่มีน้ำหนักตัวน้อยได้
เมื่อเปรียบ เทียบกับ Adult hematopoietic stem cells เซลล์ของ cord blood มีข้อดีทางชีววิทยา คือ stem cells ใน cord blood มีความสามารถใน growth proliferation มากกว่า, immune cells มีลักษณะ reactive น้อยกว่า, และมีความเสี่ยงต่อการเกิด allogeneic reactions ที่รุนแรงน้อยกว่า คุณสมบัติต่างๆ เหล่านี้ สามารถชดเชยการที่มีจำนวนเซลล์ค่อนข้างน้อยใน cord blood แต่ละ unit แต่สามารถปลูกถ่ายติดในผู้ป่วยที่ผ่านการได้รับยาเคมีบำบัดหรือการฉายรังสี ขนาดสูง (myeloablative conditioning) มาแล้ว
ธนาคารเลือดจากสายสะดือ (Umbilical cord blood banks)11,12 ได้ถูกจัดตั้งขึ้นในนานาประเทศ รวมทั้งประเทศไทย13 เพื่อเป็นแหล่งรวบรวม units ของ cord blood เพื่อการสรรหา unit ที่เหมาะสมและนำไปใช้ปลูกถ่าย unrelated donor cord blood โดยมี cord blood เก็บสะสมไว้มากกว่า 100,000 units ทั่วโลก มีการปลูกถ่าย cord blood ให้แก่ผู้ป่วยเด็กไปแล้วมากกว่า 2,500 ราย และปลูกถ่ายให้ผู้ใหญ่จำนวนหนึ่งแล้ว ทั้งผู้ป่วยโรคมะเร็ง และโรคร้ายอื่นที่ไม่ใช่มะเร็ง
ตารางที่ 1 แสดงถึงข้อดีและข้อเสียของการใช้ unrelated cord blood เพื่อการปลูกถ่าย และข้อดี ในทางปฏิบัติของการใช้ cord blood เป็น alternative source ของ stem cell แสดงในตารางที่ 2

การ ศึกษาถึงตัวบ่งชี้ทางมารดาและทารกแรกเกิดที่มีผลต่อ hematopoietic potential ของ cord blood พบว่า เด็กทารกที่มี gestational age มากจะมี cell count มากกว่า แต่มีจำนวน CD34+ cells ต่ำกว่า และมี colony-forming units-granulocyte-macrophage (CFU-GM) มากกว่า15 เด็กทารกน้ำหนักตัวมาก จะมี cell count มากกว่า มีจำนวน CD34+ cells สูงกว่า และมี CFU-GM มากกว่า
ตารางที่ 3. แสดงถึงโรคที่มีรายงานว่าสามารถรักษาหายได้ด้วยการปลูกถ่าย cord blood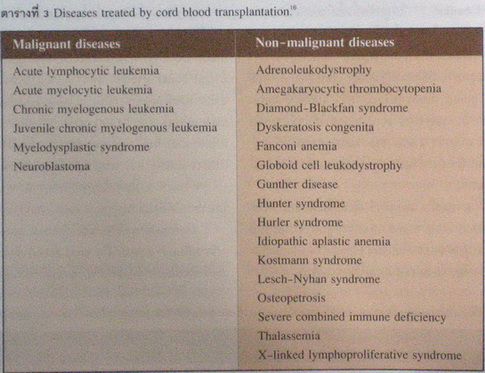
รายงานผลการศึกษาของ Surbek และคณะ17 เปรียบเทียบจำนวนเซลล์ใน cord blood ที่เก็บก่อนและหลังคลอดรก พบว่าการเก็บ cord blood ก่อนที่รกจะคลอด จะได้จำนวน nucleated cells และ CFU สูงกว่า นอกจากนี้ ยังพบว่าในการตั้งครรภ์ที่มารดาเกิดภาวะแทรกซ้อน จะได้ปริมาณ cord blood จำนวน nucleated cells และ CD34+ cells ต่ำกว่าปรกติ18 ความรู้ในเรื่องนี้มีความหมาย เพราะจำนวน nucleated cells ที่ให้ผู้ป่วยมีความสัมพันธ์กับความเร็ว ในการปลูกถ่าย neutrophil และ platelet ติดรวมถึงสัมพันธ์กับโอกาสที่จะมีชีวิตรอดในระยะยาวหลังการปลูกถ่าย19-21
ภาวะ immaturity ของระบบภูมิคุ้มกันของทารกแรกเกิด ทำให้เกิด alloreactivity ของ lymphocyte ลดลง ทำให้ลดอุบัติการและความรุนแรงของ GVHD22-24 Lymphocytes ของ cord blood มีลักษณะ naïve และ immature อุดมไปด้วย double negative CD3+ cells และสร้าง cytokines ได้น้อย Cord blood cells มีการทำงานของ natural killer (NK) และ T-cell ในระยะแรกๆ บกพร่อง แต่สามารถเกิด secondary activation ได้25 ดังนั้น GVL effect ซึ่งเป็นผลดีในการต่อต้านการกลับเป็นซ้ำของ leukemia จึงสามารถเกิดขึ้นได้ แม้ว่าการเกิด GVHD จะลดน้อยลง เนื่องจากการเกิด acute GVHD ซึ่งเป็นปรากฏการณ์ที่อาจเกิดได้ในช่วงแรกๆ หลังการปลูกถ่าย stem cell แบบ allogeneic เป็นผลมาจากการหลั่ง cytokines จึงอธิบายได้ว่า ทำไมการปลูกถ่าย umbilical cord blood จึงมีอุบัติการและความรุนแรงของ acute และ chronic GVHD น้อยกว่าการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดโลหิตจากไขกระดูก เพราะการปลูกถ่ายจากเซลล์ adult จะมีจำนวน mature T cells ปะปนมากกว่า
ข้อ พิจารณาในการคัดสรร Cord blood unit อันดับแรกคือ จำนวนของ stem cells ที่ collected ได้ต้องมีจำนวนมากเพียงพอ คำนวณจำนวนเซลล์ต่อน้ำหนักตัวของผู้รับ เพราะถ้าจำนวนเซลล์น้อยเกิน ไป ก็อาจปลูกถ่ายในตัวผู้ป่วยไม่ติด อันดับสองคือ HLA compatibility ควรหลีกเลี่ยงการปลูกถ่ายที่มี combination ของ HLA mismatches ทั้ง class I และ class II หรือมี HLA mismatches มากกว่า 2 ตำแหน่ง นอกจากว่าไม่สามารถหา cord blood unit อื่นที่เหมาะสมกว่าได้ และ unit นั้นมีจำนวน nucleated cells (mononuclear cells) มากกว่า 2.5 x 107 เซลล์/กิโลกรัม หรือจำนวน CD 34+ cells มากกว่า 1.7 x 105 เซลล์/กิโลกรัม26
ในต่างประเทศ มีการปลูกถ่ายเลือดสายสะดือแก่ผู้ป่วยผู้ใหญ่หลายราย ยกตัวอย่างการศึกษาของ Barker และคณะ27 ถึงผลการปลูกถ่ายในผู้ป่วย 608 รายซึ่งส่วนใหญ่เป็นโรคมะเร็งเม็ดเลือดขาว มีอายุตั้งแต่ 4 เดือนถึง 58 ปี (อายุเฉลี่ย 9 ปี) น้ำหนักตัว 5 ถึง 136 กิโลกรัม (น้ำหนักเฉลี่ย 30 กิโลกรัม) พบว่า จำนวน stem cell dose ที่เพียงพอและการที่เป็น HLA match เป็นปัจจัยสำคัญของการปลูกถ่ายติด (engraftment) ที่ดีและอัตราการตาย (treatment-related mortality) ที่น้อยลง
ในแง่ของข้อจำกัดของการปลูกถ่ายเลือดสายสะดือ เนื่องจากเลือดสายสะดือที่เก็บได้จากเด็กทารกแรกเกิดแต่ละคนมีปริมาณจำกัด ทำให้จำนวน stem cell dose มีน้อย อาจจะไม่เพียงพอที่จะปลูกถ่ายติดในผู้ป่วยที่มีน้ำหนักตัวมาก การค้นคว้าถึงวิธีการที่จะเพิ่มจำนวนหรือคุณภาพของเซลล์ต้นกำเนิดเม็ดโลหิต จึงมีความจำเป็น มีการศึกษากระบวนการ Ex-vivo expansion เพื่อเพิ่มจำนวน stem cells ในเลือดสายสะดือ แต่ก็พบปัญหาความสามารถในการ homing ลดลง ในกรณีการปลูกถ่ายแบบ unrelated donor ถ้าผู้ป่วยไม่สามารถมีการปลูกถ่ายติดสำเร็จ เกิดการสลัดเซลล์ของผู้ให้ (graft failure or rejection) ก็ไม่มีทางจะได้ cord blood จากเด็กทารกคนเดิมมาเพิ่มเติมหรือมาปลูกถ่ายใหม่
เพื่อหาทางแก้ไขปัญหาการมีจำนวน stem cells น้อยเกินไปที่จะปลูกถ่ายติด มีการศึกษาถึงการปลูก ถ่าย double cord blood transplantation28 โดยใช้ unrelated cord blood 2 units ปลูกถ่ายในผู้ป่วยผู้ใหญ่ซึ่งส่วนใหญ่เป็นโรคมะเร็งเม็ดเลือดขาว เกณฑ์ในการคัดเลือกคือ cord blood ทั้ง 2 units จะต้องมี HLA match กันอย่างน้อย 4 ใน 6 ตำแหน่งขึ้นไป และแต่ละ unit จะต้อง match กับผู้ป่วยอย่างน้อย 4 ใน 6 ตำแหน่งขึ้นไปด้วย ทั้งนี้ทั้ง 2 units จะต้องมีจำนวน mononuclear cells รวมกันอย่างน้อย 3.0 x 107 เซลล์/กิโลกรัมขึ้นไป Ballen และคณะ29 ได้รายงานผลการรักษาในผู้ป่วยผู้ใหญ่ 43 รายพบว่า มีอัตราการรอดชีวิต ณ 1 ปีเท่ากับร้อยละ 71 อัตราการรอดชีวิตโดยปราศจากโรค ณ 1 ปีเท่ากับร้อยละ 66
การ ปลูกถ่ายเลือดสายสะดือจากเด็กทารก ผู้บริจาคที่ไม่ใช่น้องผู้ป่วยในประเทศไทย (Unrelated donor cord blood transplantation in Thailand)
เริ่มตั้งแต่ปี พ.ศ. 2538 นพ.สุรพล อิสรไกรศีล และคณะ30 ที่โรงพยาบาลศิริราช ได้ทำการปลูกถ่ายเลือดสายสะดือรักษาผู้ป่วยเด็กโรค beta-thalassemia ได้สำเร็จเป็นรายแรกของโลก ซึ่งเป็นการใช้เลือดสายสะดือของน้อง (matched related donor) มารักษาพี่ที่ป่วย จากนั้นก็มีการปลูกถ่ายแบบ related donor เรื่อยมา
ต่อมา ตั้งแต่ปี พ.ศ. 2545 นพ.ปรีดา วาณิชยเศรษฐกุล และคณะ31 ที่โรงพยาบาลจุฬาลงกรณ์ ได้ทำการปลูกถ่ายเลือดสายสะดือแก่ผู้ป่วยเด็กไปแล้ว 15 ราย ในจำนวนนี้ 5 รายเป็นการปลูกถ่ายเลือดสายสะดือโดยใช้ Thai unrelated cord blood units ที่ถูกเก็บสะสมไว้ที่ National cord blood bank13 ของศูนย์บริการโลหิตแห่งชาติ สภากาชาดไทย โดยใช้ เพื่อรักษาผู้ป่วยเด็กโรค Wiskott-Aldrich syndrome 1 ราย โรค Beta-thalassemia/ hemoglobin E 2 ราย ซึ่งนับเป็นการปลูกถ่ายแบบ unrelated donor cord blood ประสบผล stem cells ติดสำเร็จเป็น 3 รายแรกของประเทศไทย31-34 แม้ว่าแต่ละรายจะใช้ unrelated cord blood units ที่เป็นเพียง 5 ใน 6 match ก็ตาม ส่วนผู้ป่วยเด็กรายที่ 4 เป็นโรค severe aplastic anemia และรายที่ 5 เป็นโรคมะเร็งชนิด acute lymphoblastic leukemia ซึ่งประสบผลสำเร็จในการรักษา สำหรับผู้ป่วยเด็กอีก 10 รายที่เหลือ 9 รายเป็นโรค Beta-thalassemia/ hemoglobin E35,36 ที่ได้รับ cord blood จาก related donors คือน้องของผู้ป่วยเองอีก 1 รายเป“นโรค acute leukemia การรักษาได้ผลดีเป็นส่วนใหญ่ ปลูกถ่ายสำเร็จทั้งหมด 8 รายและทำให้ผู้ป่วยหายขาดจากโรค มีเพียง 2 รายที่ไม่สำเร็จเนื่องจากมี HLA-mismatch ถึงคนละ 2-3 ตำแหน่ง (2 to 3 antigen mismatch)
อย่าง ไรก็ตาม ในแง่ภาวะแทรกซ้อนหลังการปลูกถ่ายเซลล์ติด ผู้ป่วยโรค beta-thalassemia 2 ราย มีปัญหา cutaneous GVHD grade II ซึ่งรักษาด้วย oral immunosuppressive therapy ได้ผลและหายสนิท และผู้ป่วย 1 รายซึ่งได้รับ unrelated cord blood unit เกิด acute intestinal GVHD
บทสรุป
ใน ยุคของการรักษาด้วยการปลูกถ่ายเลือดสายสะดือ มีความท้าทายและประเด็นที่จะต้องพินิจพิจารณา ทั้งทางด้านเวชศาสตร์ วิทยาศาสตร์ เทคโนโลยี จริยธรรม และระเบียบกฎเกณฑ์ต่างๆ เลือดสายสะดือมีศักยภาพที่ดีและเป็นแหล่งทางเลือกหนึ่งของการนำเซลล์ต้น กำเนิดมาใช้ประโยชน์ สามารถเลือกสรรและนำมาใช้ได้ทันที ทันเวลาที่จะช่วยผู้ป่วยที่เป็นโรคร้ายที่ไม่อาจรอผู้บริจาคบริจาคไขกระดูก ได้นานนัก ก่อนที่โรคจะกำเริบหรือคร่าชีวิตผู้ป่วยเสียก่อน ขั้นตอนการเก็บเลือดสายสะดือก็ไม่มีอันตรายหรือความยากลำบากต่อเด็กทารกแรก เกิดหรือมารดาผู้เพิ่งจะคลอดบุตร การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดโลหิตโดยใช้เลือดสายสะดือสามารถกระทำได้ผล สำเร็จ โดยเฉพาะเมื่อทำการรักษาตั้งแต่ยังอยู่ในระยะที่โรคยังไม่กำเริบรุนแรง จะได้ผลดีมาก นั่นแสดงว่า การแสวงหา Unrelated cord blood unit ที่เหมาะสม ควรรีบดำเนินการแต่เนิ่นๆ โดยเร็ว การขยายจำนวน cord blood units ที่เก็บสงวนไว้ในธนาคารเลือดสายสะดือก็เป็นสิ่งสำคัญอย่างยิ่ง เพื่อเพิ่มโอกาสให้ผู้ป่วยมี cord blood unit ที่เหมาะสมให้เลือกใช้อย่างเพียงพอ
เอกสารอ้างอิง
1. McCullough J, Hansen J, Perkins H. The National Marrow Donor Program: how it works, accomplishments to date. Oncology 1989;3:63-8;discussion 72-4.
2. Perkins HA, Hansen JA. The US National Marrow Donor Program. Am J Pediatr Hematol Oncol 1994;16(1):30-4.
3. Kernan NA, Bartsch G, Ash RC. Analysis of 462 transplantations from unrelated donors facilitated by the National Marrow Donor Program. N Engl J Med 1993;328:593-602.
4. ปรีดา วาณิชยเศรษฐกุล. Cord Blood Transplantation. ใน : สุดารัตน์ ใหญ่สว่าง, บรรณาธิการ. Medicine beyond the horizon เวชศาสตร์ร่วมสมัย 2545. กรุงเทพ- มหานคร : ภาพพิมพ์; 2545:57-66.
5. Davies SM, Kollman C, Anasetti C, et al. Engraftment and survival after unrelated donor bone marrow transplantation : a report from the National Bone Marrow Donor Program. Blood 2000;96:4096-102.
6. Sasazuki T, Juji T, Morishima Y, et al. Effect of matching of class I HLA alleles on clinical outcome after transplantation of hematopoietic stem cells from an unrelated donor. N Engl J Med 1998; 339:1177-85.
7. Petersdorf EW, Gooley TA, Anasetti C et al. Optimizing outcome after unrelated marrow transplantation by comprehensive matching of HLA class I and II alleles in the donor and the recipient. Blood 1998;92:3515-20.
8. Hansen JA, Gooley TA, Martin PJ, et al. Bone marrow transplants from unrelated donors for patients with chronic myeloid leukemia. N Engl J Med 1998;338: 962-8.
9. Speiser DE, Tiercy JM, Rufer N, et al. High resolution HLA matching associated with decreased mortality after unrelated bone marrow transplantation. Blood 1996;10: 4455-62.
10. Gluckman E, Broxmeyer HE, Auerbach AD et al. Hematopoietic reconstitution in a patient with Fanconi anemia by means of umbilical cord blood from an HLA-identical sibling. N Engl J Med 1989;321:1174-8.
11. Rubinstein P, Dobrila L, Rosenfield RE, et al. Processing and cryopreservation of placental/umbilical cord blood for unrelated bome marrow reconstitution. Proceedings of the National Academy of Sciences USA 1995;92:10119-22.
12. Rubinstein P, Rosenfield RD, Adamson JW, et al. Stored placental blood for unrelated bone marrow reconstitu-tion. Blood 1993;81:1679-90.
13. Wacharaprechanont T, O-Charoen R, Vanichsetakul P, Sudjai D, Kupatawintu P, Seksarn P, et al. Cord blood collection for the National Cord Blood Bank in Thailand. J Med Assoc Thai 2003;86(Suppl. 2):S409-16.
14. Barker JN, Krepski TP, DeFor TE, et al. Searching for unrelated donor hematopoietic stem cells: availability and speed of umbilical cord versus bone marrow. Biol Blood Marrow Transplant 2002;8:257-60.
15. Ballen KK, Wilson M, Wuu J, et al. Bigger is better : maternal and neonatal predictors of hematopoietic potential of umbilical cord blood units. Bone Marrow Transplant 2001;27:7-14.
16. Ballen K, Broxmeyer HE, McCullough J, et al. Current status of cord blood banking and transplantation in the United States and Europe. Biol Blood Marrow Transplant 2001;7:635-45.
17. Surbek DV, Visca E, Steinmann C, et al. Umbilical cord blood collection before placental delivery during cesarean delivery increases cord blood volume and nucleated cell number available for transplantation. Am J Obstet Gynecol 2000;183:218-21.
18. Surbek DV, Aufderhaar U, Holzgreve W. Umbilical cord blood collection for transplantation : which technique should be preferred? Am J Obstet Gynecol 2000;183: 1587-8.
19. Rubinstein P, Carrier C, Scaradavou A, et al. Outcomes among 562 recipients of placental blood transplants from unrelated donor. N Engl J Med 1998;339:1565-77.
20. Gluckman E, Rocha V, Boyer Chammard A, et al. Outcome of cord blood transplantation from related and unrelated donors. N Engl J Med 1997;337:373-81.
21. Kurtzberg J, Laughlin M, Graham L, et al. Placental blood as a source of hematopoietic stem cells for transplantation into unrelated recipients. N Engl J Med 1996;335:157-66.
22. De La Selle V, Gluckman E, Bruley-Rosset M. Graft versus host disease and graft versus leukemia effect in mice grafted with newborn blood. Blood 1998;92:3968-75.
23. Madrigal JA, Cohen SBA, Gluckman E, Charron DJ. Does cord blood transplantation result in lower graft versus host disease? It takes more than two to tango. Hum Immunol 1997;56: 1-5.
24. De La Selle V, Gluckman E, Bruley-Rosset M. Newborn blood can engraft adult mice without inducing graft versus host disease across non H-2 antigens. Blood 1996;87: 3977-83.
25. Gardiner CM, Meara AO, Reen DJ. Differential cytotoxicity of cord blood and bone marrow-derived natural killer cells. Blood 1998; 91:207-13.
26. Wagner JE. Umbilical cord blood transplantation: the state of the art. Scientific program of the 4th annual international umbilical cord blood transplantation symposium; May 19-20, 2006; Los Angeles, California.
27. Barker J, Scaradavou A, Stevens C, Rubinstein P. Analysis of 608 umbilical cord blood (UCB) transplants: HLA-match is a critical determinant of transplant-related mortality (TRM) in the post-engraftment period even in the absence of acute graft-versus-host disease. Scientific program of the 4th annual international umbilical cord blood transplantation symposium; May 19-20, 2006; Los Angeles, California.
28. Baker KS, Wagner JE. Double umbilical cord transplants (UCBT) with myeloablative or reduced intensity conditioning regimen (RIC). Scientific program of the 4th annual international umbilical cord blood transplantation symposium; May 19-20, 2006; Los Angeles, California.
29. Ballen K. Double cord blood transplantation in adults using a reduced intensity chemotherapy only conditioning regimen. Scientific program of the 4th annual international umbilical cord blood transplantation symposium; May 19-20, 2006; Los Angeles, California.
30. Issaragrisil S, Visuthisakchai S, Suvatte V, et al. Transplantation of cord blood stem cells into a patient with severe thalassemia. N Engl J Med 1995;332:367-9.
31. Vanichsetakul P, Wacharaprechanont T, O-Charoen R, Seksarn P, Kupatawintu P. Umbilical cord blood transplantation in children with beta-thalassemia diseases. J Med Assoc Thai 2004;87(Suppl. 2):S62-7.
32. ปรีดา วาณิชยเศรษฐกุล. การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดโลหิตจากอาสาสมัครผู้บริจาคสำเร็จที่โรง พยาบาลจุฬาลงกรณ์ Successful Unrelated Donor Stem Cell Transplantation at King Chulalongkorn Memorial Hospital. ใน : สุดารัตน์ ใหญ่สว่าง, สิริชัย ปาสาทิกา, ปานฉัตร ภัครัชพันธุ์, บรรณาธิการ. เวชศาสตร์ร่วมสมัย 2547. กรุงเทพมหานคร: ภาพพิมพ์; 2547:87-90.
33. Vanichsetakul P, O-Charoen R, Seksarn P, Kupatawintu P. Outcome of pediatric hematopoietic stem cell transplantations from Thai unrelated donors matched with high-resolution HLA typing. J Med Assoc Thai 2005;88(Suppl. 4):S1-6.
34. Vanichsetakul P, Seksarn P, Wacharaprechanont T, O-Charoen. Unrelated versus related donors cord blood transplantation for children with non-malignant hematologic diseases. Abstract presented in the 48th annual meeting of American Society of Hematology, December 9-12, 2006; Orlando, Florida, U.S.A.
35. Vanichsetakul P, Wacharaprechanont T, Sucharitchan P, Seksarn P, O-Charoen R. Successful cord blood transplantation in thalassemia major patient at King Chulalongkorn Memorial Hospital. Chula Med J 2003;47(7):411-8.
36. Vanichsetakul P, Seksarn P, Nuchprayoon I. Stem cell transplantation from HLA-identical siblings versus alternative donors in beta-thalassemia diseases. Abstract presented in the 48th annual meeting of American Society of Hematology, December 9-12, 2006; Orlando, Florida, U.S.A.
ปรีดา วาณิชยเศรษฐกุล พ.บ.
รองศาสตราจารย์, หน่วยโลหิตวิทยา
ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย
ไม่มีความคิดเห็น:
แสดงความคิดเห็น